Dyspnée chez un chien qui régurgite
Chienne Beauceron de 6 ans cachectique, en dyspnée, avec toux et régurgitation, la réponse est-elle évidente pour vous ?
Dr vétérinaire Charlotte Gillot, assistante d’imagerie médicale
Dr vétérinaire Charlotte Vallin, assistante de médecine interne
Dr vétérinaire Anaïs COMBES, DipECVDI, PhD, EBVS European Specialist in Veterinary Diagnostic Imaging
Une chienne Beauceron femelle entière de 6 ans est présentée pour toux et dysphagie évoluant depuis 2 mois et vomissements/régurgitations quotidiens évoluant depuis 2 semaines.
L’examen clinique révèle une cachexie (Note d’état corporel 1/5), un abattement, une douleur à la palpation abdominale et une dyspnée mixte avec dominante expiratoire.
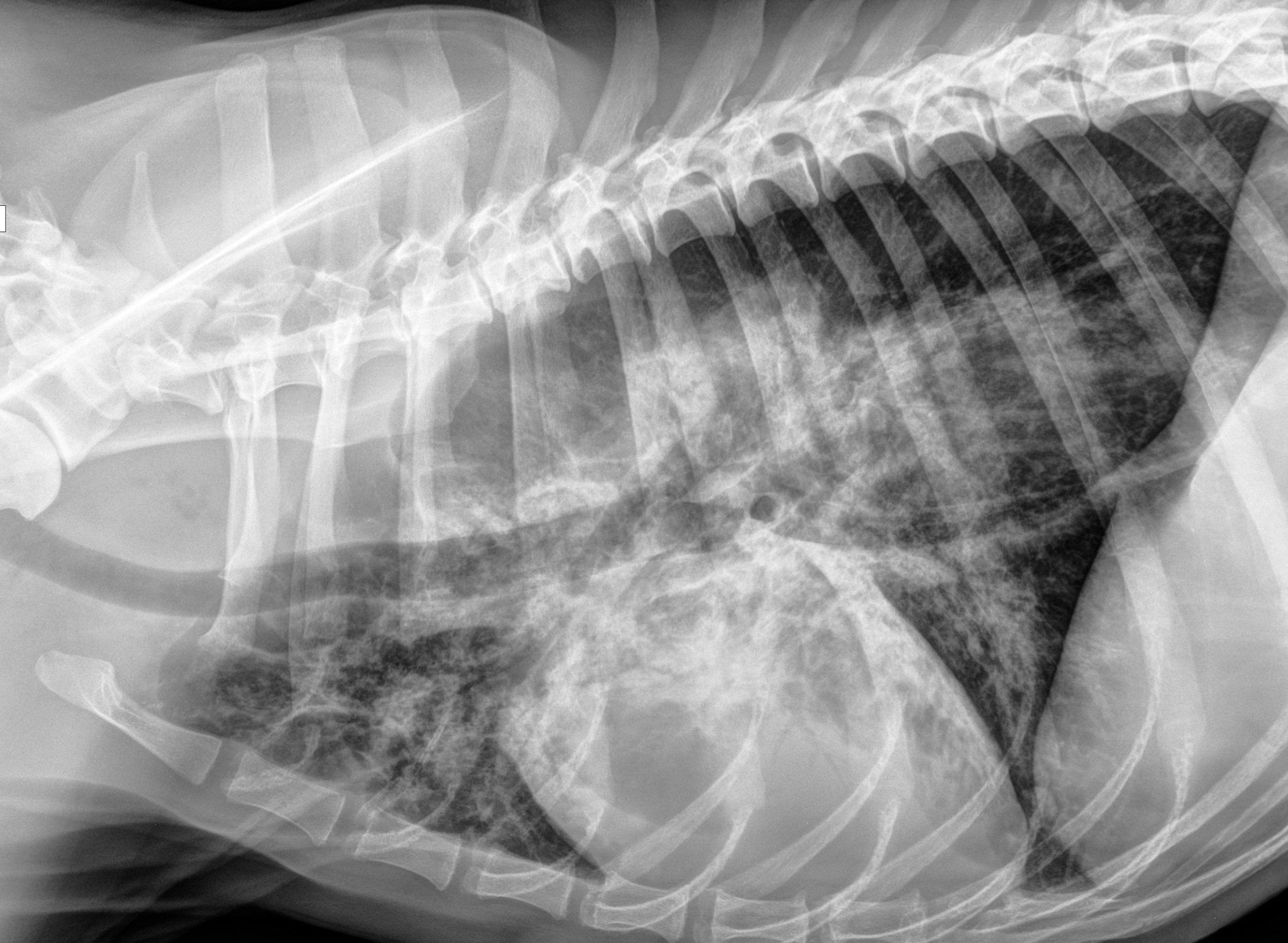
Des radiographies thoraciques sont réalisées (photos 1a & 1b).

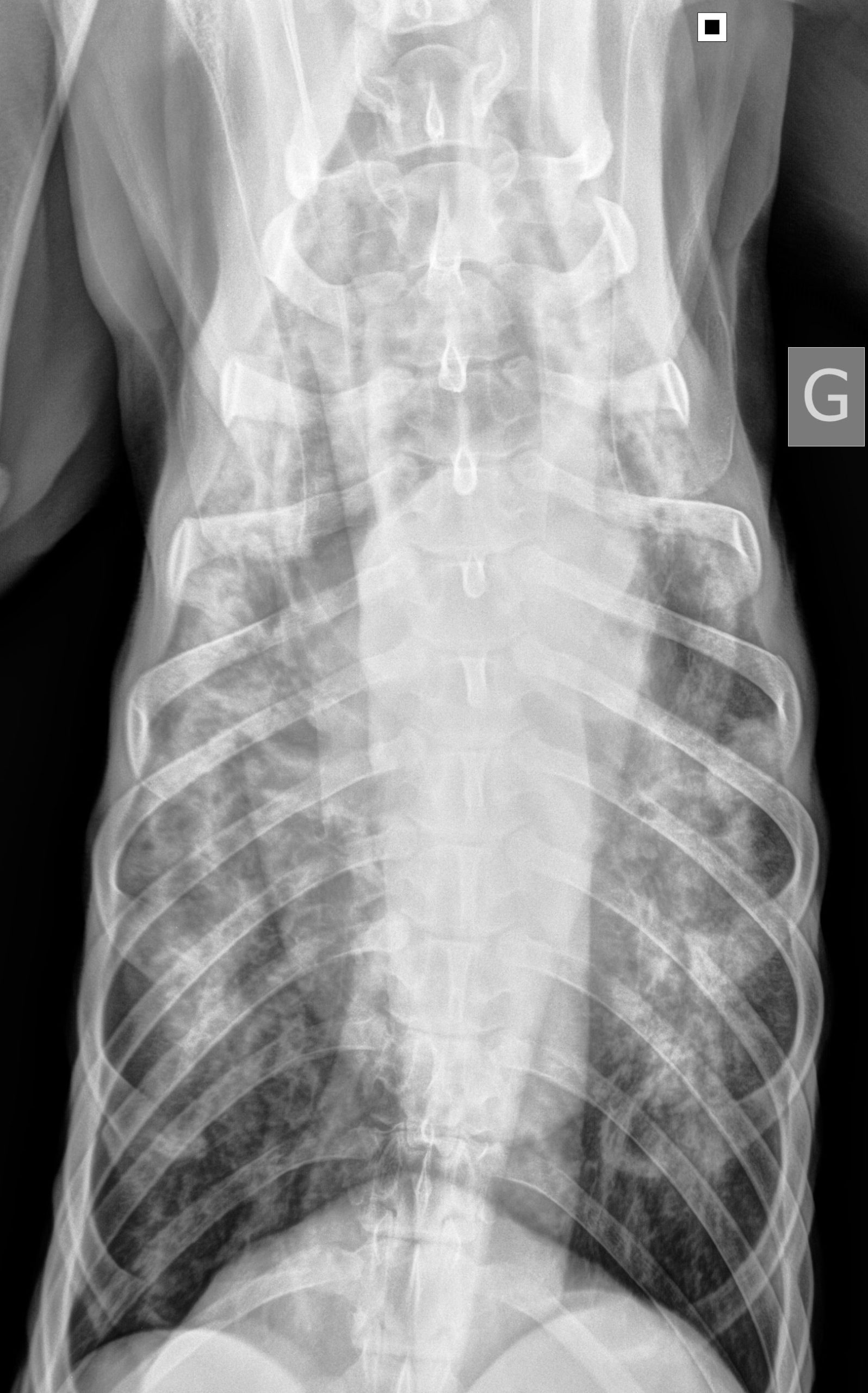

Quelles anomalies radiographiques observez-vous ?
On note un effacement de bord gauche de la silhouette cardiaque sur la projection ventrodorsale, une opacification augmentée dans les lobes pulmonaires craniaux droit et gauche, moyen droit et caudal gauche, une perte de visualisation des vaisseaux pulmonaires et des bronchogrammes aériques et un signe lobaire du lobe caudal gauche (sur la projection latérale). Ces lésions sont compatibles avec une consolidation pulmonaire lobaire multifocale ventrale.
Le reste du parenchyme pulmonaire présente également une opacification bronchique avec des images en anneaux et en rails, sévère cranialement et discrète caudalement.
Enfin, on note une dilatation gazeuse marquée de l’œsophage thoracique, se manifestant par :
- Le signe de la bande trachéale
- Une déviation ventrale de la trachée et de la silhouette cardiaque
- Un élargissement du médiastin crânial et caudal par une opacité gazeuse, entouré par deux lignes d’opacité tissulaire (correspondant à la paroi œsophagienne) qui convergent au niveau du sphincter œsophagien caudal
- Des bulles de gaz dans la région anatomique de l’œsophage en région cervicale caudale
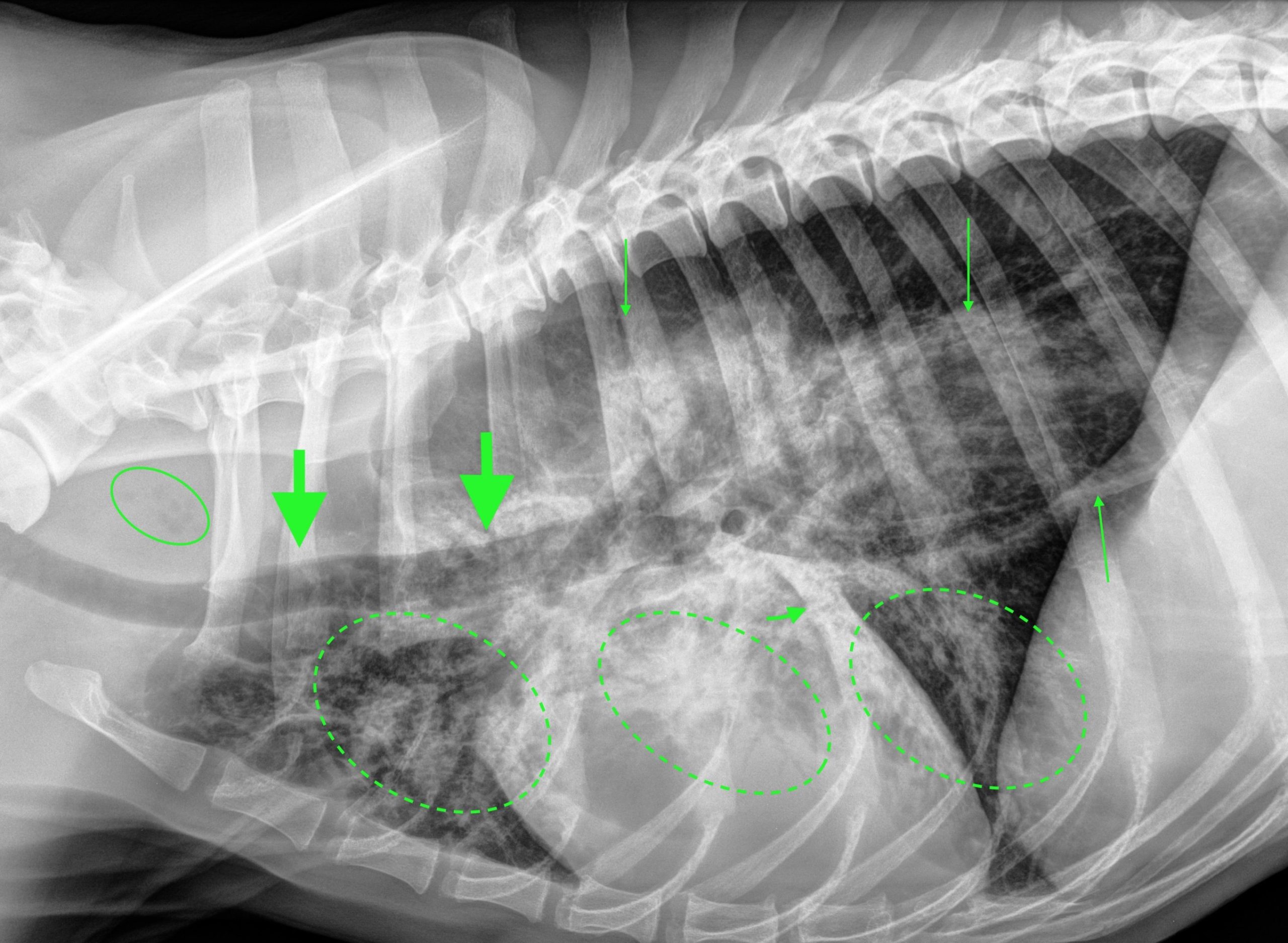
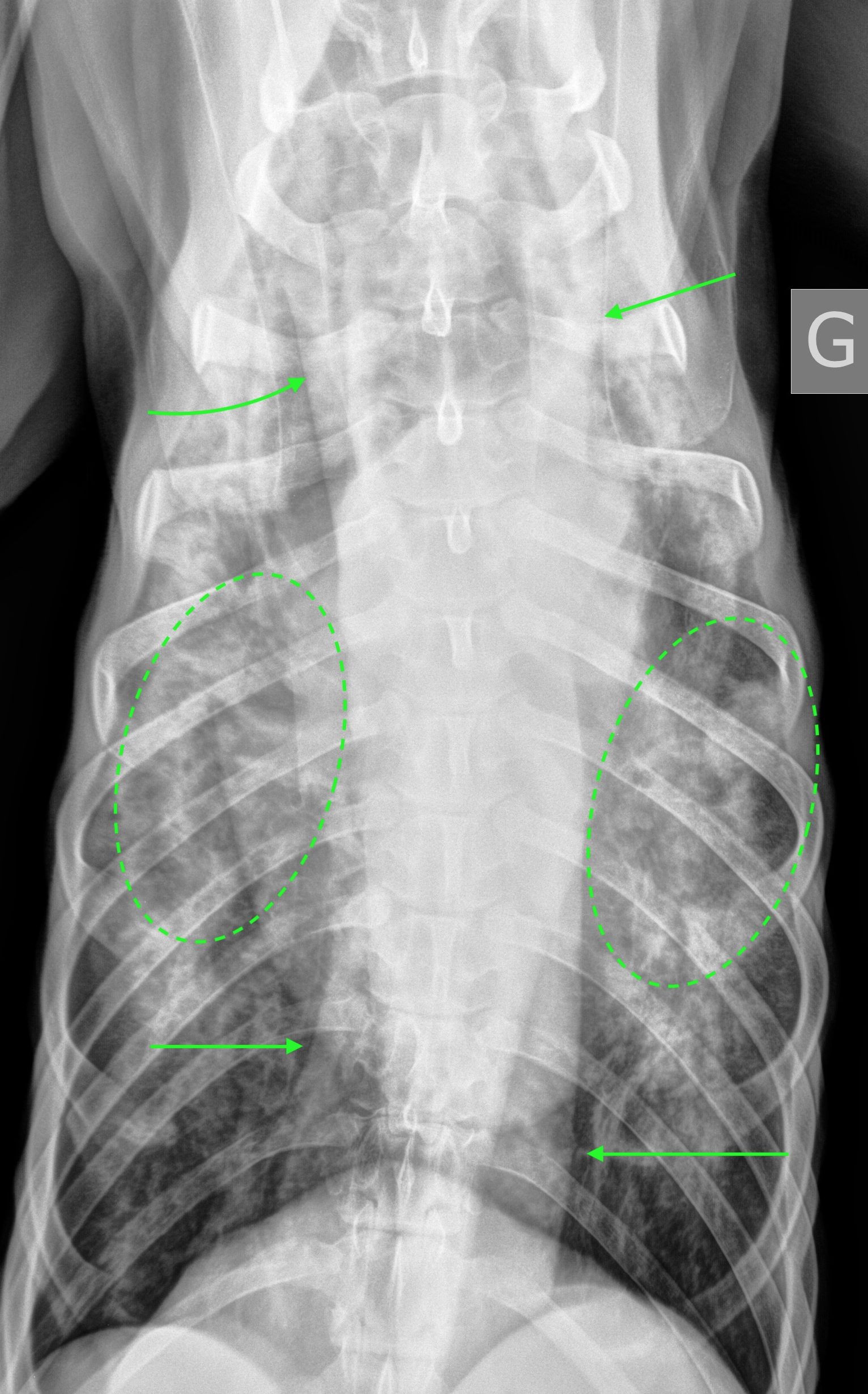
Quelles sont les hypothèses diagnostiques ?
La consolidation pulmonaire ventrale bilatérale lobaire et l’opacification bronchique sont compatible prioritairement avec une bronchopneumonie par fausse déglutition, secondaire à la dilatation œsophagienne sévère. Cette dilatation généralisée peut avoir une origine fonctionnelle (mégaoesophage idiopathique ou congénital, troubles neuromusculaires, œsophagite) ou moins probablement mécanique (obstruction œsophagienne distale) (1).
Quelle prise en charge proposeriez-vous ?
Dans un cas de dilatation oesophagienne, il convient d’affiner les différentes hypothèses diagnostiques.
Une endoscopie digestive par voie haute (œso-gastro-duodénoscopie) serait indiquée afin d’objectiver les lésions œsophagiennes : œsophagite, présence d’une sténose œsophagienne, d’un diverticule œsophagien, d’une masse œsophagienne ou une persistance du quatrième arc aortique (2) et gastrique : gastrite, reflux gastro-oesophagien.
En parallèle, une exploration des causes secondaires du méga-œsophage peut être effectuée selon les signes cliniques : une hypothyroïdie, un hypocorticisme ou encore une myasthénie grave (3).
Des affections plus rares peuvent également être responsables d’un méga-œsophage comme une intoxication au plomb, aux organophosphorés, un lupus érythémateux disséminé, une dermatomyosite ou une polymyopathie.
Dans notre cas, les premières investigations ont permis de mettre en évidence des signes de gastrite. Une oesophagite secondaire par reflux a été suspectée, sans pouvoir exclure une autre origine. L’état clinique instable du patient n’a pas permis de le confirmer grâce, en particulier, à une endoscopie ou d’autres examens complémentaires sous anesthésie générale.
Concernant la prise en charge médicale, elle reçoit des traitements digestifs de soutien (maropitant, sucralfate, pantoprazole, métoclopramide), une fluidothérapie adaptée à sa déshydratation, une antibiothérapie large spectre (amoxiciline-acide clavulanique) ainsi qu’une alimentation en hauteur en plusieurs repas journaliers.
Malgré la mise en place des traitements, notre patient continue de présenter de nombreuses régurgitations et une aggravation de la bronchopneumonie est suspectée. La pose d’une sonde de gastrotomie percutanée (4) aurait pu être envisagée (limitation des régurgitations et réalimentation de l’animal), mais au vu de la dégradation de l’état général et des difficultés respiratoires, une décision de fin de vie est prise par les propriétaires.
Bibliographie
- Thrall DE, ed. 7th.Section IV. In: Textbook of Veterinary Diagnostic Radiology (Seventh Edition). W.B. Saunders; 2018, p. 606.
- Ettinger SJ, « Disorders of the Esophagus ». In: Textbook of Veterinary Internal Medicine (Eighth Edition). Saunders; 2017.
- Mignan T, Targett M, Lowrie M. Classification of myasthenia gravis and congenital myasthenic syndromes in dogs and cats. Vol. 34, Journal of Veterinary Internal Medicine. Blackwell Publishing Inc.; 2020. p. 1707–17.
- Kuz’min-Krutetskiĭ MI, Demko AE, Safoev AI, Akkalaeva A, Karimova LI. [Percutaneous endoscopic gastrostomy]. Vestn Khir Im I I Grek. 2014;173(3):19–23.
Pour aller plus loin dans les affections du système nerveux périphérique, voici une description des indications de l’électrodiagnostic en Neurologie Vétérinaire.
Actualités associées
Faire une IRM sur votre animal en Nouvelle Aquitaine : c’est possible !
Les radiologues spécialistes d'Alliance réalisent et interprètent des…

La dysplasie du coude chez le chien
Le terme de « dysplasie » est un terme général qui pourrait êtr…

Du nouveau pour votre clinique vétérinaire Alliance
Avec un nouvel établissement dédié à la médecine spécialisée et a…